Page 5 - พันธะไอออนิก
P. 5
8
2. อะตอมของอโลหะ มีคาอิเล็กโทรเนกาติวิตี (EN) สูง จะรับอิเล็กตรอนเขามาใหครบ 8 ที่วง
ี
ิ
ี
็
นอกสุดแลวกลายเปนไอออนลบที่มีการจัดเรยงอเลกตรอนที่เสถยรคลายแกสเฉอย มีประจุ
ื่
ไฟฟาเปนลบเทากับจํานวนอิเล็กตรอนที่รับ ดังนี้
หมู VIIA จะรับ 1 อิเล็กตรอน แลวกลายเปนไอออนที่มีประจุไฟฟา 1- เชน Cl -
หมู VIA จะรับ 2 อิเล็กตรอน แลวกลายเปนไอออนที่มีประจุไฟฟา 2- เชน S 2-
หมู VA จะรับ 3 อิเล็กตรอน แลวกลายเปนไอออนที่มีประจุไฟฟา 3- เชน N 3-
ั
หมู IVA สวนใหญไมสรางพนธะไอออนิก ถาจะสรางพันธะแบบไอออนิกจะให
ิ
ุ
ั
็
อเลกตรอน 4 อเลกตรอนหรออาจรบ 4 อเล็กตรอน ดงนั้นจึงมีประจเปน 4+ หรอ 4-
ิ
ั
ื
ื
็
ิ
4+
เชน C หรือ C 4-
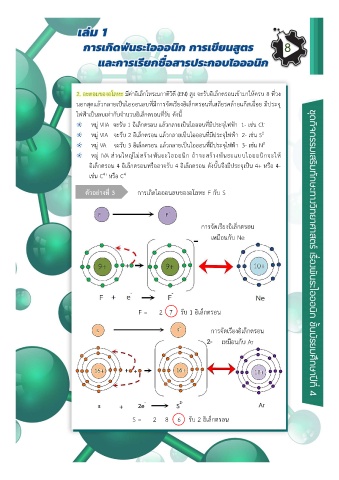
ตัวอยางที่ 3 การเกิดไอออนลบของอโลหะ F กับ S
การจัดเรียงอิเล็กตรอน
เหมือนกับ Ne
F = 2 7 รับ 1 อิเล็กตรอน
การจัดเรียงอิเล็กตรอน
เหมือนกับ Ar
S = 2 8 6 รับ 2 อิเล็กตรอน