Page 45 - Hybrid PBD 2022 Tg 5 - Kimia
P. 45
Kimia Tingkatan 5 Bab 3
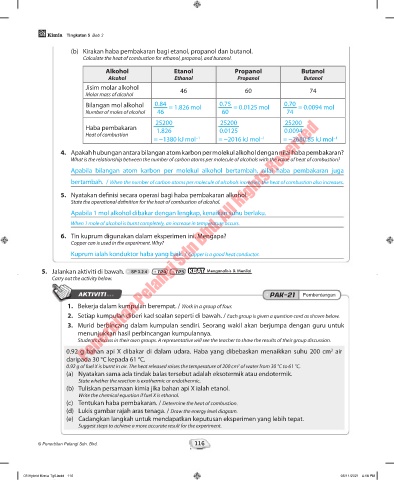
(b) Kirakan haba pembakaran bagi etanol, propanol dan butanol.
Calculate the heat of combustion for ethanol, propanol, and butanol.
Alkohol Etanol Propanol Butanol
Alcohol Ethanol Propanol Butanol
Jisim molar alkohol 46 60 74
Molar mass of alcohol
Bilangan mol alkohol 0.84 = 1.826 mol 0.75 = 0.0125 mol 0.70 = 0.0094 mol
Number of moles of alcohol 46 60 74
Penerbitan Pelangi Sdn Bhd. All Rights Reserved
25200 25200 25200
Haba pembakaran 1.826 0.0125 0.0094
Heat of combustion
= −1380 kJ mol −1 = −2016 kJ mol −1 = −2680.85 kJ mol −1
4. Apakah hubungan antara bilangan atom karbon per molekul alkohol dengan nilai haba pembakaran?
What is the relationship between the number of carbon atoms per molecule of alcohols with the value of heat of combustion?
Apabila bilangan atom karbon per molekul alkohol bertambah, nilai haba pembakaran juga
bertambah. / When the number of carbon atoms per molecule of alcohols increases, the heat of combustion also increases.
5. Nyatakan definisi secara operasi bagi haba pembakaran alkohol.
State the operational definition for the heat of combustion of alcohol.
Apabila 1 mol alkohol dibakar dengan lengkap, kenaikan suhu berlaku.
When 1 mole of alcohol is burnt completely, an increase in temperature occurs.
6. Tin kuprum digunakan dalam eksperimen ini. Mengapa?
Copper can is used in the experiment. Why?
Kuprum ialah konduktor haba yang baik. / Copper is a good heat conductor.
5. Jalankan aktiviti di bawah. SP 3.2.4 TP4 TP5 KBAT Menganalisis & Menilai
Carry out the activity below.
AKTIVITI PAK-21 Pembentangan
1. Bekerja dalam kumpulan berempat. / Work in a group of four.
2. Setiap kumpulan diberi kad soalan seperti di bawah. / Each group is given a question card as shown below.
3. Murid berbincang dalam kumpulan sendiri. Seorang wakil akan berjumpa dengan guru untuk
menunjukkan hasil perbincangan kumpulannya.
Students discuss in their own groups. A representative will see the teacher to show the results of their group discussion.
0.92 g bahan api X dibakar di dalam udara. Haba yang dibebaskan menaikkan suhu 200 cm air
3
daripada 30 °C kepada 61 °C.
3
0.92 g of fuel X is burnt in air. The heat released raises the temperature of 200 cm of water from 30 °C to 61 °C.
(a) Nyatakan sama ada tindak balas tersebut adalah eksotermik atau endotermik.
State whether the reaction is exothermic or endothermic.
(b) Tuliskan persamaan kimia jika bahan api X ialah etanol.
Write the chemical equation if fuel X is ethanol.
(c) Tentukan haba pembakaran. / Determine the heat of combustion.
(d) Lukis gambar rajah aras tenaga. / Draw the energy level diagram.
(e) Cadangkan langkah untuk mendapatkan keputusan eksperimen yang lebih tepat.
Suggest steps to achieve a more accurate result for the experiment.
© Penerbitan Pelangi Sdn. Bhd. 116
03 Hybrid Kimia Tg5.indd 116 05/11/2021 4:18 PM