Page 147 - กำหนดการสอน-ว31104-วิทยาศาสตร์กายภาพ-ม.5
P. 147
126
2-
2+
(MgSO ) เมื่อละลายน้ าจะอยู่ในรูปของแมกนีเซียมไอออน (Mg ) กับซัลเฟตไอออน (SO ) ตัวอย่าง
4
4
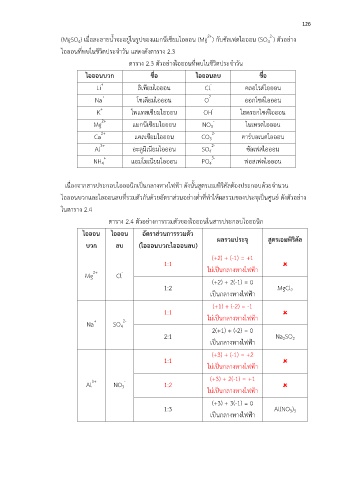
ไอออนที่พบในชีวิตประจ าวัน แสดงดังตาราง 2.3
ตาราง 2.3 ตัวอย่างไอออนที่พบในชีวิตประจ าวัน
ไอออนบวก ชื่อ ไอออนลบ ชื่อ
+
-
Li ลิเทียมไอออน Cl คลอไรด์ไอออน
+
2-
Na โซเดียมไอออน O ออกไซด์ไอออน
+
-
K โพแทสเซียมไอออน OH ไฮดรอกไซด์ไอออน
2+
-
Mg แมกนีเซียมไอออน NO ไนเทรตไอออน
3
2+
2-
Ca แคลเซียมไอออน CO คาร์บอเนตไอออน
3
2-
Al 3+ อะลูมิเนียมไอออน SO ซัลเฟสไอออน
4
3-
+
NH แอมโมเนียมไอออน PO ฟอสเฟตไอออน
4
4
เนื่องจากสารประกอบไอออนิกเป็นกลางทางไฟฟูา ดังนั้นสูตรเอมพิริคัลต้องประกอบด้วยจ านวน
ไอออนบวกและไอออนลบที่รวมตัวกันด้วยอัตราส่วนอย่างต่ าที่ท าให้ผลรวมของประจุเป็นศูนย์ ดังตัวอย่าง
ในตาราง 2.4
ตาราง 2.4 ตัวอย่างการรวมตัวของไอออนในสารประกอบไอออนิก
ไอออน ไอออน อัตราส่วนการรวมตัว ผลรวมประจุ สูตรเอมพิริคัล
บวก ลบ (ไอออนบวก:ไอออนลบ)
(+2) + (-1) = +1
1:1
-
2+
Mg Cl ไม่เป็นกลางทางไฟฟูา
(+2) + 2(-1) = 0
1:2 MgCl
2
เป็นกลางทางไฟฟูา
(+1) + (-2) = -1
1:1 ไม่เป็นกลางทางไฟฟูา
2-
+
Na SO 2(+1) + (-2) = 0
4
2:1 Na SO
2
2
เป็นกลางทางไฟฟูา
(+3) + (-1) = +2
1:1
ไม่เป็นกลางทางไฟฟูา
(+3) + 2(-1) = +1
3+
-
Al NO 1:2
3
ไม่เป็นกลางทางไฟฟูา
(+3) + 3(-1) = 0
1:3 Al(NO )
3 3
เป็นกลางทางไฟฟูา