Page 47 - เคมีสำหรับครู 2
P. 47
เคมีสำหรับครู 2 (Chem. for teachers 2) 23
ตัวอย่างที่ 1.8 | การรบกวนสมดุลเคมโดยการเปลี่ยนความเข้มข้น
ี
โจทย์ : จากปฏิกิริยา
3+
-
2 Fe (aq) + 2 l(aq) ⇌ 2 Fe (aq) + l2(g)
2+
เมื่อระบบอยู่ในสภาวะสมดุล เมื่อเติมสารต่าง ๆ เหล่านี้ลงไปจะเกิดการเปลี่ยนแปลงอย่างไร
สารที่เติม : (a) Fe(NO3)3 (b) FeCl2 (c) KI (d) NaCl (e) NH4I (f) LiI (g) AgNO3
วิธีคิด ในตัวอย่างนี้เราจะเฉลยแนวทางและวิธีคิดสรุปได้ดังตาราง
ทิศทางการ ความเข้มข้นของสารที่สมดุลใหม่
ข้อ สารที่เติม รบกวนโดยการ เปลี่ยนแปลงของสมดุล Fe l Fe l2
2+
-
3+
3+
(a) Fe(No30)3 เพิ่ม Fe → เพิ่ม ลด เพิ่ม เพิ่ม
2+
(b) FeCl2 เพิ่ม Fe ← เพิ่ม เพิ่ม เพิ่ม ลด
-
(c) KI เพิ่ม I → ลด เพิ่ม เพิ่ม เพิ่ม
(d) NaCl ไม่มีผลต่อทิศทางสมดุลของปฏิกิริยา
-
(e) NH4I เพิ่ม I → ลด เพิ่ม เพิ่ม เพิ่ม
-
(f) LiI เพิ่ม I → ลด เพิ่ม เพิ่ม เพิ่ม
-
ลด I
-
+
(g) AgNO3 โดยที่ Ag จะจับกับ I เกิดเป็น ← เพิ่ม ลด ลด ลด
ตะกอนของ AgI เสมือนเป็นการ
ดึง I ออกจากระบบ
-
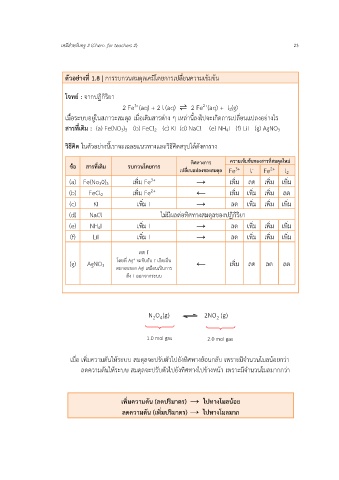
เมื่อ เพิ่มความดันให้ระบบ สมดุลจะปรับตัวไปยังทิศทางย้อนกลับ เพราะมีจำนวนโมลน้อยกว่า
ลดความดันให้ระบบ สมดุลจะปรับตัวไปยังทิศทางไปข้างหน้า เพราะมีจำนวนโมลมากกว่า
เพิ่มความดัน (ลดปริมาตร) → ไปทางโมลน้อย
ลดความดัน (เพิ่มปริมาตร) → ไปทางโมลมาก