Page 18 - ชุดกิจกรรมอัตราการเกิดปฏิกิริยาเคมี
P. 18
18
ิ
ั
1. ปฏิกริยำเคมีต่ำงชนิดกัน พลงงำนกระตุ้นก็ต่ำงกัน
ิ
2. ปฏิกริยำที่มีพลังงำนกระตุ้นต่ ำ เกิดได้เร็วกว่ำปฏิกริยำที่มีพลังงำนกระตุ้นสูง
ิ
3. พลังงำนกระตุ้นไม่เกี่ยวข้องกับอัตรำกำรเกิดปฏิกิริยำ
ิ
4. พลังงำนกระตุ้นไม่เกี่ยวข้องกับพลังงำนของปฏิกริยำ (∆E)
5. พลังงำนกระตุ้นของปฏิกิริยำหนึ่งๆเป็นค่ำเฉพำะตัว อำจมีกำรเปลี่ยนแปลงได้ ถ้ำมีสำรบำงชนิดเข้ำ
ไปร่วมในปฏิกิริยำ
4. พลังงานกับการด าเนินไปของปฏิกิริยา
พลังงานกับการด าเนินไปของปฏิกิริยา
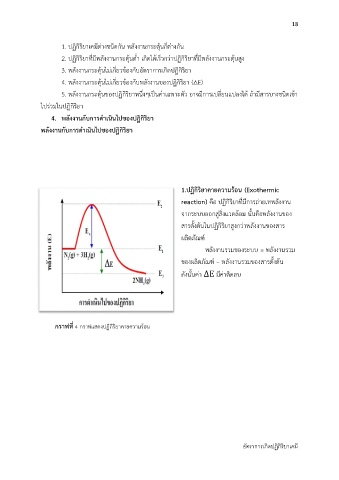
1.ปฏิกิริยาคายความร้อน (Exothermic
reaction) คือ ปฏิกริยำที่มีกำรถ่ำยเทพลังงำน
ิ
จำกระบบออกสู่สิ่งแวดล้อม นั้นคือพลังงำนของ
ิ
สำรตั้งต้นในปฏิกริยำสูงกว่ำพลังงำนของสำร
ผลิตภัณฑ์
พลังงำนรวมของระบบ = พลังงำนรวม
ั
ของผลิตภัณฑ์ – พลงงำนรวมของสำรตั้งต้น
ดังนั้นค่ำ ∆E มีค่ำติดลบ
กราฟที่ 4 กรำฟแสดงปฏิกิริยำคำยควำมร้อน
ิ
ิ
อัตราการเกดปฏิกริยาเคมี