Page 815 - ตำราเคมีอินทรีย์ [Jadsada Ratniyom]
P. 815
เคมีอินทรีย์ (Org. Chem.) 787
หากวงเบนซีนของอะนีลีนมีหมู่แทนที่ที่ให้อิเล็กตรอนเกาะอยู่ เช่น pCH3-C6H5NH2
(p-methylaniline) หมู่ให้คือหมู่ CH3 จะให้อิเล็กตรอนแบบอินดักทีฟ ทำให้ความหนาแน่นของ
อิเล็กตรอนบนไนโตรเจนอะตอมสูงขึ้น ความเป็นเบสของ pCH3-C6H5NH2 จึงสูงกว่า อะนีลีน
CH3 ให้อิเล็กตรอนแบบอินดักทีฟ ทำให้ความ
เป็นเบสของ NH2 มากขึ้น
ดังนั้น ความเป็นเบสของอัลริลลามีนจึงสรุปได้ดังแสดงด้านล่าง
ความเป็นเบสเพิ่มขึ้น
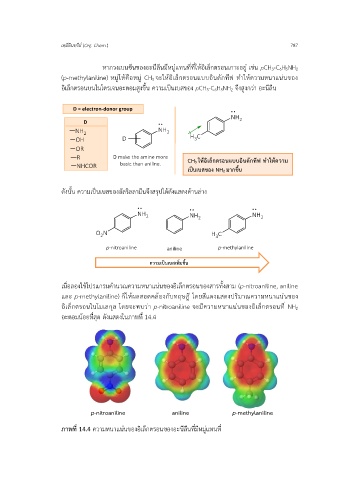
เมื่อลองใช้โปรแกรมคำนวณความหนาแน่นของอิเล็กตรอนของสารทั้งสาม (p-nitroaniline, aniline
และ p-methylaniline) ก็ให้ผลสอดคล้องกับทฤษฎี โดยสีแดงแสดงปริมาณความหนาแน่นของ
อิเล็กตรอนในโมเลกุล โดยจะพบว่า p-nitroaniline จะมีความหนาแน่นของอิเล็กตรอนที่ NH2
อะตอมน้อยที่สุด ดังแสดงในภาพที่ 14.4
p-nitroaniline aniline p-methylaniline
ภาพที่ 14.4 ความหนาแน่นของอิเล็กตรอนของอะนีลีนที่มีหมู่แทนที่